Colegio de Ciencias y Humanidades
Plantel Vallejo
Materia:
Química
Alumna:
Romero Reyes Yessica Paola
Profesor:
Gregorio
Grupo 171 A
Tema:
Lluvia Acida, sus efectos sobre el medio y los seres vivos, reacciones químicas que lo originan.
Lluvia acida
Se denomina lluvia acida a un tipo de desastre natural caracterizado por la precipitación pluvial que, según estudios bioquímicos, presenta un pH o grado de acidez menor a 5.65 (atención: también puede presentarse como nieve, niebla, roció, etc.). Esto es así porque las sustancias químicas que se encuentran suspendidas en la atmósfera precipitan junto con el agua. La mayoría de estas sustancias acidas provienen de las centrales térmicas aunque también están presentes los resultantes de la combustión de combustibles fósiles como por ejemplo aquellos utilizados en los motores a explosión. Este problema ecológico se remonta a los inicios de la Revolución Industrial, incrementando los niveles de smog acido desde ese momento que por mecanismos eólicos (vientos) son depositados o transferidos a zonas alejadas no industrializadas. El comienzo de los estudios y la denuncia de este problema, por pertenecer a un área ampliamente afectada, son los países del norte de Europa.
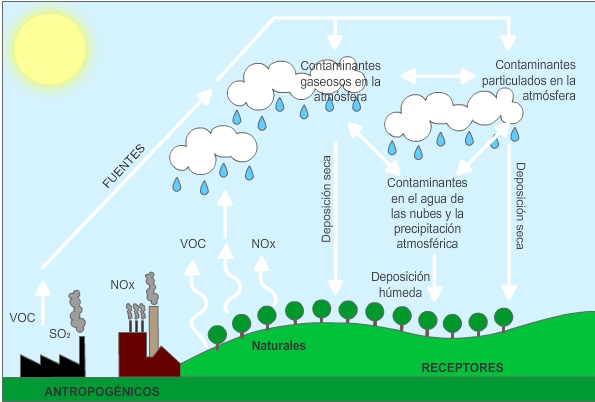
Formación de la lluvia ácida
- Una gran parte del SO2 (dióxido de azufre) emitido a la atmósfera procede de la emisión natural que se produce por las erupciones volcánicas, que son fenómenos irregulares. Sin embargo, una de las fuentes de SO2 es la industria metalúrgica. El SO2 puede proceder también de otras fuentes, por ejemplo como el sulfuro de dimetilo, (CH3)2S, y otros derivados, o como sulfuro de hidrógeno, H2S. Estos compuestos se oxidan con el oxígeno atmosférico dando SO2. Finalmente el SO2 se oxida a SO3 (interviniendo en la reacción radicales hidroxilo y oxígeno) y este SO3 puede quedar disuelto en las gotas de lluvia, es el de las emisiones de SO2 en procesos de obtención de energía: el carbón, el petróleo y otros combustibles fósiles contienen azufre en unas cantidades variables (generalmente más del 1%), y, debido a la combustión, el azufre se oxida a dióxido de azufre.
S + O2 → SO2
Los procesos industriales en los que se genera SO2, por ejemplo, son los de la industria metalúrgica. En la fase gaseosa el dióxido de azufre se oxida por reacción con el radical hidroxilo por una reacción intermolecular.
SO2 + OH· → HOSO2· seguida por HOSO2· + O2 → HO2· + SO 3
En presencia del agua atmosférica o sobre superficies húmedas, el trióxido de azufre (SO3) se convierte rápidamente en ácido sulfúrico (H2SO4).
SO3(g) + H2O (l) → H2SO4(l)
- El NO se forma por reacción entre el oxígeno y el nitrógeno a alta temperatura.
O2 + N2 → 2NO
Una de las fuentes más importantes es a partir de las reacciones producidas en los motores térmicos de los automóviles y aviones, donde se alcanzan temperaturas muy altas. Este NO se oxida con el oxígeno atmosférico,
O2 + 2NO → 2NO2, y este 2NO2
y reacciona con el agua dando ácido nítrico (HNO3), que se disuelve en el agua.
3NO2 + H2O → 2HNO3 + NO
Causas de la lluvia acidaLos componentes tóxicos que forman la lluvia acida son el dióxido de azufre y el oxido de nitrógeno provenientes de la combustión del carbón o de hidrocarburos. Mediante una serie de reacciones químicas, el dióxido de azufre se transforma en trióxido de azufre que a su vez y a través de algunos catalizadores ambientales o bien por la acción directa de la luz solar, se transforma en acido sulfúrico provocando importantes daños ambientales al regresar a la tierra a través de la lluvia acida. |
Consecuencias provocadas por la lluvia acida |
La lluvia acida genera severos daños ambientales y de ahí su importancia desde el punto de vista ecológico. Sin lugar a dudas, existen diferencias entre algunos ecosistemas que los hacen mas susceptibles que otros. Las características biológicas de los suelos mas afectados son: los formados por partículas gruesas sobre principalmente granito, de poca profundidad y no calcáreos, presentan poca capacidad de procesar la materia orgánica lo cual genera que toda sustancia que ingresa al ecosistema sea eliminada de forma pausada. Debemos pensar que además del daño producido a través de la tierra existe un daño directo sobre los elementos vegetales producidos por los tóxicos presentes en la lluvia acida.
uno de los ecosistemas mas afectados por la lluvia acida son los acuáticos y en especial aquellos de agua dulce. Esto es así porque cuando se depositan los tóxicos presentes en la lluvia acida generan una disminución del pH del agua y los seres vivos que habitan dentro (peces, crustáceos y plantas acuáticas) no soportan niveles de acidez mayores a un pH de 5. Esto provoca irremediablemente la muerte de ellos e incluso algunos lagos del norte de Europa se ha descrito que han quedado totalmente estériles (sin presencia de organismos vivos) luego de la contaminación por lluvia acida.
Soluciones
Entre las medidas que se pueden tomar para reducir la emisión de los contaminantes precursores de éste problema tenemos las siguientes:
Reducir el nivel máximo de azufre en diferentes combustibles.
Trabajar en conjunto con las fuentes fijas de la industria para establecer disminuciones en la emisión de SOx y NOx, usando tecnologías para control de emisión de estos óxidos.
Impulsar el uso de gas natural en diversas industrias.
Introducir el convertidor catalítico de tres vías.
La conversión a gas en vehículos de empresas mercantiles y del gobierno.
Ampliación del sistema de transporte eléctrico.
Instalación de equipos de control en distintos establecimientos.
No agregar muchas sustancias químicas en los cultivos.
Adición de un compuesto alcalino en lagos y ríos para neutralizar el pH.
Control de las condiciones de combustión (temperatura, oxigeno, etc.).
No hay comentarios:
Publicar un comentario