Universidad Nacional Autónoma de México
Colegio de Ciencias y Humanidades
Plantel Vallejo
Nombre del alumno: García Pérez Paola
Nombre del Profesor: Gregorio
Grupo: 171- A
N.L: 6
Tema: Lluvia Ácida
Lluvia ácida

La lluvia ácida se forma cuando la
humedad en el
aire se combina con los
óxidos de nitrógeno y el
dióxido de azufre emitidos por fábricas, centrales eléctricas y vehículos que queman
carbón o productos derivados del
petróleo. En interacción con el
vapor de agua, estos gases forman
ácido sulfúrico y
ácidos nítricos. Finalmente, estas sustancias químicas caen a la tierra acompañando a las
precipitaciones, constituyendo la lluvia ácida.
Los contaminantes atmosféricos primarios que dan origen a la lluvia ácida pueden recorrer grandes distancias, siendo trasladados por los vientos cientos o miles de kilómetros antes de precipitar en forma de rocío, lluvia, llovizna, granizo, nieve, niebla o neblina. Cuando la precipitación se produce, puede provocar importantes deterioros en el ambiente.
La lluvia normalmente presenta un
pH de aproximadamente 5.65 (ligeramente ácido), debido a la presencia del CO2 atmosférico, que forma
ácido carbónico, H2CO3. Se considera lluvia ácida si presenta un pH de menos de 5 y puede alcanzar el pH del
vinagre (pH 3). Estos valores de pH se alcanzan por la presencia de ácidos como el
ácido sulfúrico, H2SO4, y el
ácido nítrico, HNO3. Estos ácidos se forman a partir del
dióxido de azufre, SO2, y el monóxido de nitrógeno que se convierten en ácidos.
Los hidrocarburos y el carbón usados como fuente de energía, en grandes cantidades, pueden también producir óxidos de
azufre y
nitrógeno y el
dióxido de azufre emitidos por fábricas, centrales eléctricas y vehículos que queman
carbón o productos derivados del
petróleo.
Efectos de la lluvia ácida
La
acidificación de las aguas de lagos, ríos y mares dificulta el desarrollo de vida acuática en estas aguas, lo que aumenta en gran medida la mortalidad de peces. Igualmente, afecta directamente a la vegetación, por lo que produce daños importantes en las zonas forestales, y acaba con los
microorganismos fijadores de N.
El termino "lluvia ácida" abarca la
sedimentación tanto húmeda como seca de contaminantes ácidos que pueden producir el deterioro de la superficie de los materiales. Estos contaminantes que escapan a la atmósfera al quemarse carbón y otros componentes fósiles reaccionan con el agua y los oxidantes de la atmósfera y se transforman químicamente en ácido sulfúrico y nítrico. Los compuestos ácidos se precipitan entonces a la tierra en forma de lluvia, nieve o niebla, o pueden unirse a partículas secas y caer en forma de sedimentación seca.
La lluvia ácida por su carácter corrosivo, corroe las construcciones y las infraestructuras. Puede disolver, por ejemplo, el
carbonato de calcio, CaCO3, y afectar de esta forma a los monumentos y edificaciones construidas con
mármol o
caliza.
Un efecto indirecto muy importante es que los
protones, H+, procedentes de la lluvia ácida arrastran ciertos
iones del suelo. Por ejemplo,
cationes de hierro, calcio, aluminio, plomo o zinc. Como consecuencia, se produce un empobrecimiento en ciertos nutrientes esenciales y el denominado estrés en las plantas, que las hace más vulnerables a las
plagas.
Los
nitratos y
sulfatos, sumados a los cationes
lixiviados de los suelos, contribuyen a la
eutrofización de ríos y lagos, embalses y regiones costeras, lo que deteriora sus condiciones ambientales naturales y afecta negativamente a su aprovechamiento.
Un estudio realizado en
2005 por
Vincent Gauci[1] de
Open University, sugiere que cantidades relativamente pequeñas de
sulfato presentes en la lluvia ácida tienen una fuerte influencia en la reducción de gas
metano producido por
metanógenos en áreas pantanosas, lo cual podría tener un impacto, aunque sea leve, en el
efecto invernadero.
[2]
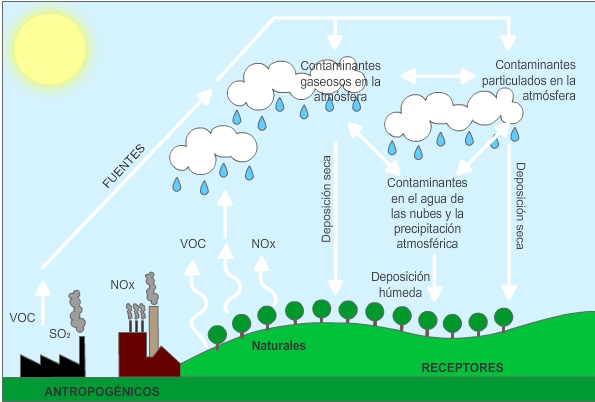
Formación de la lluvia ácida
Una gran parte del SO2 (dióxido de azufre) emitido a la atmósfera procede de la emisión natural que se produce por las
erupciones volcánicas, que son fenómenos irregulares. Sin embargo, una de las fuentes de SO2 es la
industria metalúrgica. El SO2 puede proceder también de otras fuentes, por ejemplo como el sulfuro de dimetilo, (CH3)2S, y otros derivados, o como sulfuro de hidrógeno, H2S. Estos compuestos se
oxidan con el oxígeno atmosférico dando SO2. Finalmente el SO2 se oxida a SO3 (interviniendo en la reacción radicales hidroxilo y oxígeno) y este SO3 puede quedar disuelto en las gotas de lluvia, es el de las emisiones de SO2 en procesos de obtención de energía: el carbón, el petróleo y otros combustibles fósiles contienen azufre en unas cantidades variables (generalmente más del 1%), y, debido a la combustión, el azufre se oxida a dióxido de azufre.
S + O2 → SO2
Los procesos industriales en los que se genera SO2, por ejemplo, son los de la industria metalúrgica. En la fase
gaseosa el dióxido de azufre se oxida por reacción con el radical hidroxilo por una reacción intermolecular.
SO2 + OH· → HOSO2· seguida por HOSO2· + O2 → HO2· + SO 3
En presencia del agua atmosférica o sobre superficies húmedas, el trióxido de azufre (SO3) se convierte rápidamente en
ácido sulfúrico (H2SO4).
SO3(g) + H2O (l) → H2SO4(l)
El NO se forma por reacción entre el oxígeno y el nitrógeno a alta temperatura.
O2 + N2 → 2NO
Una de las fuentes más importantes es a partir de las reacciones producidas en los
motores térmicos de los automóviles y aviones, donde se alcanzan temperaturas muy altas. Este NO se oxida con el oxígeno atmosférico,
O2 + 2NO → 2NO2, y este 2NO2
y reacciona con el agua dando
ácido nítrico (HNO3), que se disuelve en el agua.
3NO2 + H2O → 2HNO3 + NO
Soluciones
Entre las medidas que se pueden tomar para reducir la emisión de los contaminantes precursores de éste problema tenemos las siguientes:
Reducir el nivel máximo de azufre en diferentes combustibles.
Trabajar en conjunto con las fuentes fijas de la industria para establecer disminuciones en la emisión de SOx y NOx, usando tecnologías para control de emisión de estos óxidos.
Impulsar el uso de
gas natural en diversas industrias.
Introducir el
convertidor catalítico de tres vías.
La conversión a gas en vehículos de empresas mercantiles y del gobierno.
Ampliación del sistema de
transporte eléctrico.
Instalación de equipos de control en distintos establecimientos.
No agregar muchas
sustancias químicas en los cultivos.
Adición de un
compuesto alcalino en lagos y ríos para neutralizar el pH.
Control de las condiciones de combustión (temperatura, oxigeno, etc.).
Conclusión
La Lluvia Ácida a sido un problema latente desde hace varios años y en especial se ha ido agravando en esta ultima década por el crecimiento de la industria ya que estas ultimas contaminan en gran medida al medio ambiente y al hombre que vive en él , el problema con esto es que el crecimiento de la industria nos afecta mas y mas , a la sociedad y a la naturaleza.
Opinión Personal:
Uso de la Tecnología: El uso de la tecnología me parece muy favorecedor para la sociedad ya que tenemos mas posibilidades de aprovechamiento en ciertos puntos, aunque no se debe usar para todas las cosas.
El Cuidado de la Naturaleza: Todos debemos cuidarla ya que es esencial para vivir, Tenemos un planeta maravilloso y muy productivo que debemos aprovechar al máximo.